吴南屏教授团队在猴痘病毒拮抗天然免疫的研究中取得重要进展
近日,济南微生态生物医学省实验室常务副主任吴南屏教授团队在猴痘病毒拮抗天然免疫的研究中取得重要进展,研究成果以“Monkeypox virus protein OPG188 antagonizes cGAS-STING antiviral signaling pathway to mediate immune evasion”为题,在《PNAS》杂志在线发表。团队报道了猴痘病毒重要毒力蛋白OPG188拮抗cGAS-STING抗病毒信号通路,实现免疫逃逸。这项研究不仅揭示了猴痘病毒逃逸抗病毒免疫的作用机制,更为开发针对性抗病毒药物提供了全新靶点。
猴痘病毒(monkeypox virus,MPXV)的全球性传播构成了严重的公共卫生威胁。一项2024年11月发表于《JAMA》的调查研究显示,仅2022年7月至2023年5月,全球118个国家就有超过99000人感染MPXV。为此,世界卫生组织于2024年8月14日第二次宣布猴痘疫情为“国际关注的突发公共卫生事件”。
cGAS-STING通路是人体抵御DNA病毒入侵的第一道防线。当病毒DNA进入细胞质,传感器cGAS便利用ATP和GTP合成第二信使2'3'-cGAMP,该分子激活内质网上的STING蛋白,进而招募TBK1激酶磷酸化转录因子IRF3,最终启动I型干扰素(IFN-I)及下游抗病毒基因的表达。然而,MPXV作为胞质复制的DNA病毒,却演化出多种逃避免疫监视的策略。此前研究对MPXV抑制cGAS-STING的具体分子机制知之甚少,这也成为制约疫苗与药物研发的瓶颈。
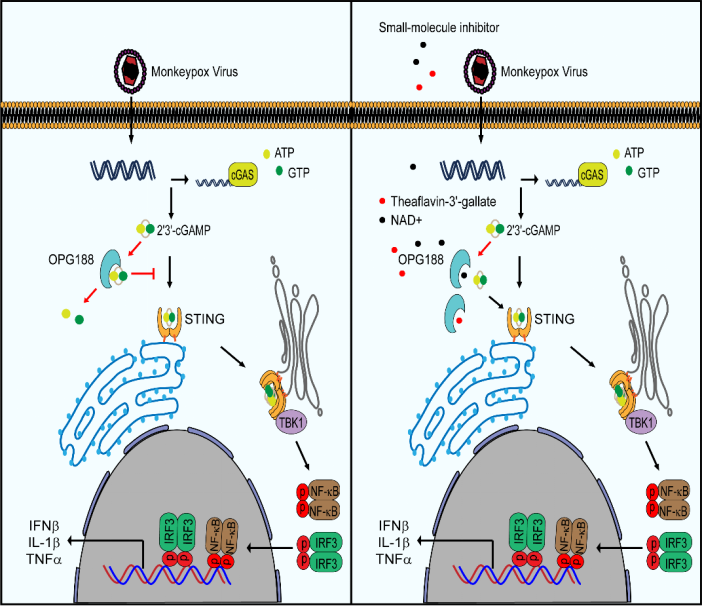
猴痘病毒OPG188拮抗cGAS-STING作用机制图
为破解这一谜题,研究团队构建了包含MPXV全基因组179个基因的表达文库,在HEK293T细胞中系统筛选能抑制cGAS-STING驱动IFN-β启动子活化的病毒蛋白。结果精准锁定三个关键“罪魁”:OPG147、OPG188和OPG200。其中,研究团队通过对OPG188发挥功能的机制进行了探究发现OPG188可在体外高效降解2′3′-cGAMP,导致细胞内2′3′-cGAMP水平下降,阻断STING从内质网向高尔基体的转运,从而切断下游信号级联。
基于OPG188催化口袋的三维结构,团队开展了大规模虚拟筛选:对FDA库2858种和TargetMol库4279种共7155个小分子进行分子对接与高通量验证。脱颖而出的两款化合物-NAD⁺(β-烟酰胺腺嘌呤二核苷酸)和茶黄素-3′-没食子酸酯(TF2B)-能竞争性结合Poxin活性口袋,显著抑制OPG188的核酸酶活性。未来,通过对这些化合物的结构进行优化,有望开发出高效抗猴痘病毒感染的药物。
科研启发
在未来的研究中,团队将依托药物筛选平台筛选针对OPG188以及其他病毒靶点的小分子药物,同时对筛选出的药物进行结构优化,这对后续抗病毒药物的开发以及病毒疫情的防控均具有重要意义。
本文第一作者为微生态与疾病研究方向创新团队的潘召义博士。